
|
|
|
Generalitati:
Coroziunea reprezinta fenomenul de distrugere partiala sau totala a materialelor in general si a metalelor in special, in urma unor reactii chimice si electrochimice, care au loc prin interactiunea materialelor cu mediul coroziv.
Protectia anticorosiva reprezinta totalitatea masurilor care se aplica pentru reducerea coroziunii si a efectelor sale la limite acceptabile din punct de vedere tehnico-economic. Nu exista o metoda universala de protectie anticorosiva. Protejarea constructiilor metalice se poate realiza actionand in doua directii:
1.prin crearea artificiala a unor obstacole cinetice
- inhibarea reactiei anodice sau a celei catodice;
- izolarea metalului de mediul corosiv prin starturi protectoare.
2.prin asigurarea unei stabilitati termodinamic a metalelore modificand valoarea potentialului de electrod al sistemului metal-mediu coroziv.
Defectoscopia nedistructiva cuprinde metode si procedee de investigare a materialelor folosite atunci cand instalatiile sau sistemele sunt in functiune si fara a afecta structura sau proprietatiile acestora.
Aspecte economice ale coroziunii
Coroziunea este o problema de interes general la fel ca sanatatea publica si protectia. Importanta si actualitatea coroziunii sunt consecinte rezultate din consumurile mari de material si energie concomitant cu cresterea poluarii mediului. Incepand din 1960 la nivel mondial s-au facut determinari si aprecieri asupra impactului economic al coroziunii. In Romania coroziunea nu a fost studiata ca efect a implicatilor tehnico-economince in totalitatea ei, ci s-au facut numai unele studii partiale privind costurile coroziunii.
Pierderi prin coroziune
In fiecare secunda pe glob se distrug prin coroziune 100 kg de otel adica anual se pierde cam 30% din intreaga productie de otel. In majoritatea tarilor costurile totale generate de coroziune (pierderile materiale), intretinerea instalatilor, protectia anticoroziva si pregatirea specialistilor se exprima in % din PIB al fiecarei tari. Exemple:- Australia cheltuieste 2%; Franta 2,8%; Germania 3%; Anglia 3,2%, Japonia 3,5%, China 4%, SUA 4,5%.
Domeniile care implica cheltuieli ridicate cu coroziunea, in SUA sunt:
-utilitatiile 34%;
-transportul 22%;
-infrastructura 16%;
-productia si fabricatia 13%.
Pierderiile totale in infrastructura sunt distribuite astfel:
-poduri rutiere 37%;
-conducte transport 31%;
-acumulare de produse periculoase 31%.
Costurile implicate de coroziune au o component din ce in ce mai mare care merge in directia educatiei, cercetarii si dezvoltarii.
Strategiile de prevenire a coroziunii
Noile tehnologii asigura metode din ce in ce mai eficiente de prevenire a coroziunii, dar sunt necesare si masuri de imbunatatire a managementului coroziunii.
Principalele directii strategice sunt cunoasterea costurilor coroziunii si indicarea posibilitatiilor de reducere a acestora:
-schimbarea compectiei ca nu se poate preveni coroziunea;
-aplicarea unor politici, reguli, standard si practice de management pentru micsorarea costurilor;
-imbunatatirea educarii si antrenarii personalului implicat impotriva coroziunii;
-dezvoltatea cercetarii si implementarea de noi tehnologii in domeniul coroziunii si a protectiei anticorozive.
Clasificarea proceselor de coroziune
Se poate face dupa mai multe criteri:
I)Dupa mecanismul reactiei de coroziune se disting 3 tipuri:
1)Coroziune chimica(in gaze) este generata de reactii in gaze uscate in special la temperaturi ridicate si in solutii de neelectroliti. Se desfasoara fara schimb de sarcini electrice si fara generare de curent electric. Se supune legiilor de baza ale cineticii reactiilor chimice eterogene. In urma coroziunii chimice pe suprafata metalului se formeaza de regula o pelicula solida si aderenta care in anumite cazuri are chiar rol de protective anticoroziva.
2)Coroziune electro-chimica(in medii umede) se produce in solutii apoase de electroliti, in gaze umede, in sol sau in electroliti topiti. Reactia de corodare are loc pe baza schimbului de sarcini electrice si este insotita de generarea unui current electric. Se supune legiilor de baza ale cineticii electro-chimice.
3)Coroziune bio-chimica sau bio-coroziunea este provocata de activitatea vitala, metabolic sau excretori a unor microorganisme. Insoteste coroziunea electro-chimica si se intalneste la instalatii ce lucreaza in zone mlastinoase sau in soluri umede.
II)Dupa distributia atacului pe suprafata metalului
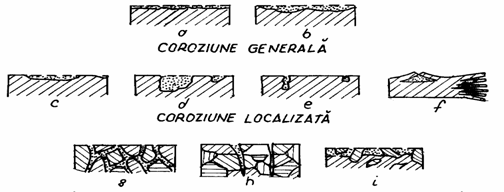
1)Coroziunea generala (continua) poate fi:
a)Coroziune uniforma cand atacul corosiv se inregistreaza pe intreaga suprafata, distrugand materialul pe aceeasi adancime.
b)Coroziune neuniforma atunci cand distrugerea are loc pe intreaga suprafata, dar pe adancimi variabile.
2)Coroziune localizata sau discontinua cu atac pe anumite zone ale suprafetei:
c)Coroziune sub forma de petec;
d)Coroziune in plagi;
e)Coroziune in puncte(pitting);
f)Coroziune sub forma de pungi.
III)Dupa caracterul distrugerii in raport cu structura metalului
g)Coroziunea intercristalina (intergranulara) cand atacul coroziv are loc de preferinta la limita grauntilor cristalini. Ca efect slabeste coroziunea cristalelor, provoaca pierderi in greutate si reduce rezistenta mecanica.
h)Coroziune intracristalina (transcristalina) distruge grauntele cristalin in integritatea sa. Efectul ei este amplificat de solicitarile mecanice, de tensiunile interne si cele termice aplicate materialelor.
i)Coroziunea selective cand atacul coroziv se manifesta numai asupra anumitor faze din structura cristalina.
IV)Coroziunea in conditii specifice
1)Coroziunea atmosferica este cea mai intalnita forma de distrugere a metalelor deoarece peste 80% din instalatii functioneaza in atmosfera. Se desfasoara in majoritatea cazurilor dupa mecanismul electro-chimic deoarece atmosfera este umeda. Principalii compusi corozivi din atmosfera sunt SO2, H2S, CO, CO2, oxizii de azot, etc.
2)Coroziunea in sol prezenta la conducte, cabluri, rezervoare, total sau partial ingropate si influentata de sarurile si O2 dizolvat in sol si de conductibilitatea electrica a solului.
3)Coroziunea microbiologica este fenomenul de distrugere a metalelor sub actiunea microorganismelor (bacterii).
4)Coroziunea in prezenta solicitarilor mecanice
Tipul de coroziune caracterizat prin forma, intindere si viteza de reactive este determinat de :
-natura materialului si a agentului coroziv;
-temperatura;
-presiune;
-viteza de curgere a fluiduluicoroziv.
Cauzele care provoaca coroziune sunt de 2 tipuri:
I)Cauze endogene - proprii materialului supus corodarii cum ar fii:
-gradul de prelucrare a suprafetelor;
-prezenta neomogenitatilor structurale si a tensiunilor interne.
II)Cauze exogene proprii factorilor externi:
-gradul de agresivitate in care lucreaza instalatia;
-conceperea unor cuplaje galvanice din material diferite;
-existenta unor asamblari neetanse si a unor zone cu grad diferit de aerare.
In cazul materialelor metalice si in special a otelurilor se constata ca alierea acestora poate sa mareasca sau sa micsoreze rezistenta la coroziune.
Metale care cresc rezistenta la coroziune a otelurilor:
-moilbden;
-crom;
-nichel.
Metale care nu influenteaza rezistenta la coroziune:
-mangan(Mn);
-Niobiu(nb).
Carbonul in cantitati mari micsoreaza rezistenta la coroziune a otelurilor aliate.
Bazele teoretice ale coroziunii
1)Coroziunea chimica - metalele se corodeaza dupa un proces chimic cand sunt in contac gaze agresive in lipsa umiditatii si in general la temperature ridicate sau in contact cu solutii de electroliti. Este un process de oxidare care se desfasoara dupa reactia generala:
![]()
Factorii care influenteaza coroziunea chimica se impart in 2 categorii:
a)Factori cu actiune intensive: natura si compozitia fazei metalice si a agentului coroziv, temperatura (mareste viteza procesului si accelereaza difuzia agentului corosiv la suprafata metalului) si durata procesului;
b) Factori care modifica viteza procesului, cum sunt: deformatiile si incluziunile superficiale ale metalului si viteza de deplasare a mediului corosiv.
Coroziunea electrochimica
Reprezinta atacul distructiv exercitat asupra metalelor sau aliajelor de catre mediul corosiv prin intermediul unor reactii chimice care implica un transfer de ioni si electroni sub influenta unei diferente de potential electric.
Procesul electrochimic de coroziune se desfasoara dupa o reactive de tip redox prin desfasurarea simultana a celor 2 fenomene (oxidare si reducere) legate intre ele printr-un bilant riguros de electricitate:
-reactia de
oxidare a metalului este o reactive anodica de ionizare :![]()
-reactia de
reducere este o reactie catodica de preluare a electronilor si trecerea ionilor
in solutie. Substanta care preia electronii se numeste depolarizant (D) si are
rolul de acceptor de electroni.![]() (ion depolarizant).
(ion depolarizant).
Concret in functie de natura mediului coroziv reactia de reducere se desfasoara astfel:
a)in mediu
acid are loc reducerea ionilor de hidrogen: ![]()
b)in mediu
alcalin are loc reducerea oxigenului dizolvat in electrolit:![]()
c)in mediu neutru are loc reducerea ionilor metalici prezenti in solutie.
Factori care influenteaza coroziunea electrochimica
Natura materialului
Metalele au potential electro-chimic mai mic decat potentialul de polarizare catodica, se corodeaza mai repede. Metalele pure si omogene sunt mai rezistente la coroziunea electro-chimica, iar aliajele cu structura de solutie solida sunt mai stabile.
Starea suprafetei
Prezenta oxigenului molecular in solutiile corozive aerate, are rol complex si se manifesta in 2 directii contradictorii astfel:
-la concentratii mici si medii oxigenul intensifica procesul de coroziune prin polarizare catodica
-la concentratii mari oxigenul actioneaza ca agent pasivizator si formeaza pelicule protectoare pe suprafata metalului.
Cand concentratia de oxigen variaza de-a lungul suprafetei metalice se produce coroziunea prin aerare diferentiata.
Metode de testare si evaluare a coroziuni
I)Metode directe:
1)Optice:-examinarea cu ajutorul ochiului liber (se distinge coroziunea uniforma, localizata, in pitting)
-examinarea cu lupa
-examinarea cu microscopul (matalografic, electronic, protonic - se determina coroziunea de tip structural)
2)Masurarea variatiei de masa (±Δm)
Exprimarea coroziunii se face in
acest caz prin indicele gravimetric ![]()
Unde:
S - suprafata corodata;
t - timpul de expunere la coroziune;
3)Masurarea volumului de gaze rezultate din coroziune cand exprimarea se face prin indicele volumetric.
In cazul cand din reactive se degaja hidrogen se masoara volumul de hidrogen (kV(H2)). In cazul in care se consuma oxigen se masoara volumul de oxigen (kV(O2))
Indicele
volumetric va avea urmatoarea expresie: ![]()
unde:
A - masa atomica a metalului;
Z - valenta ionului metal;
Cu ambii
indici gravimetric sau volumetric se poate exprima coroziune sub forma
indicelui de penetratie ![]()
4)Masurarea grosimii probei inainte si dupa corodare
II)Metode directe
1)Metode electro-chimice constau in masurarea:
-intensitatii curentului de coroziune;
-potentialului stationar de coroziune;
-trasarea curbelor de polarizare.
2)Metode mecanice.Se fac masuratori inainte si dupa coroziune pentru unele proprietati mecanice (rezistenta la rupere, incovoiere, oboseala, la soc, duritate, etc)
3)Analiza spectrala stabileste structura si compozitia produsilor de coroziune.
4)Masuratori electrice. Deoarece produsii de coroziune au rezistivitate electrica mai mare decat metalele se poate aprecia efectele coroziunii prin masurarea unor parametrii electrici.
5)Analiza chimica poate determina consumul de agent coroziv dintr-um mediu dat